近日,美国病理学家协会(College of American Pathologists,以下简称“CAP”)开展的肿瘤游离DNA高通量测序检测项目血浆游离DNA( Cell-Free DNA,cfDNA) (CFDNA-B 2020)结果公布,裕策生物旗下深圳裕康医学检验实验室(以下简称:裕康医学实验室)以满分成绩通过该类室间质评!
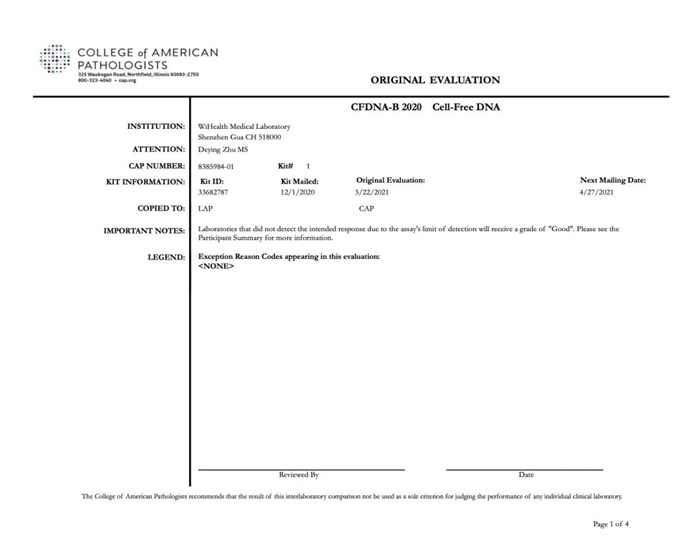
CAP CFDNA-B能力评估项目是CAP开展的评估实验室基于液体活检技术检测和分析基因变异能力的验证项目。本次质评活动检测对象为3个不同的模拟血浆样本,所用检测方法适用于血浆、脑脊液、胸腔积液和尿液等液体活检样本类型。本次检测包括BRAF、EGFR、IDH1、KRAS、NRAS等基因的15个常见突变位点,突变丰度(Variant Allele Fraction,VAF)范围设定为0.1%-1%,参评实验室需汇报最低检测限(Limit of Detection ,LOD)及检出突变的突变丰度。CAP CFDNA-B 2020能力评估结果公布,裕策生物所有检测结果均为“GOOD”,满分通过,准确率100%,无任何一例假阴性或假阳性。
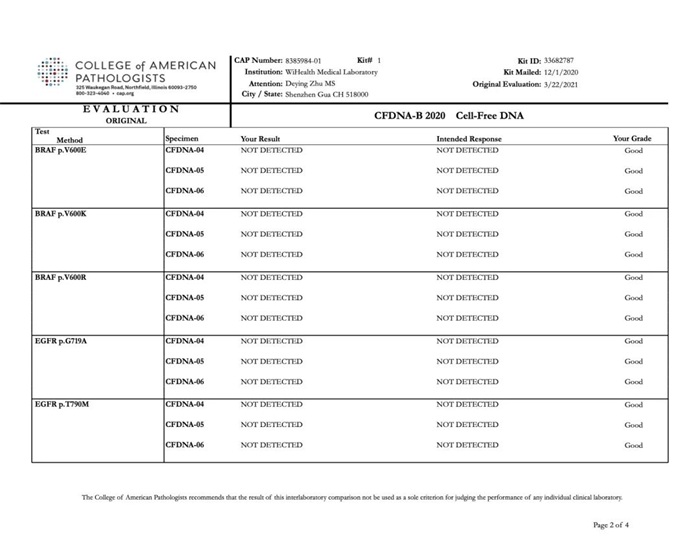
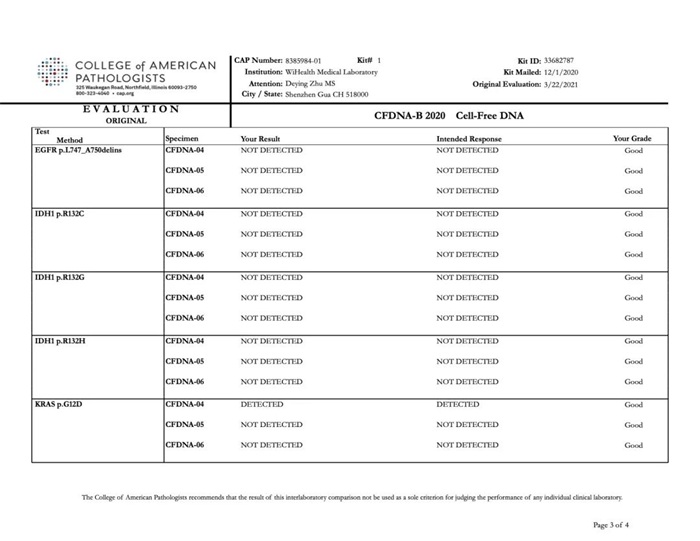
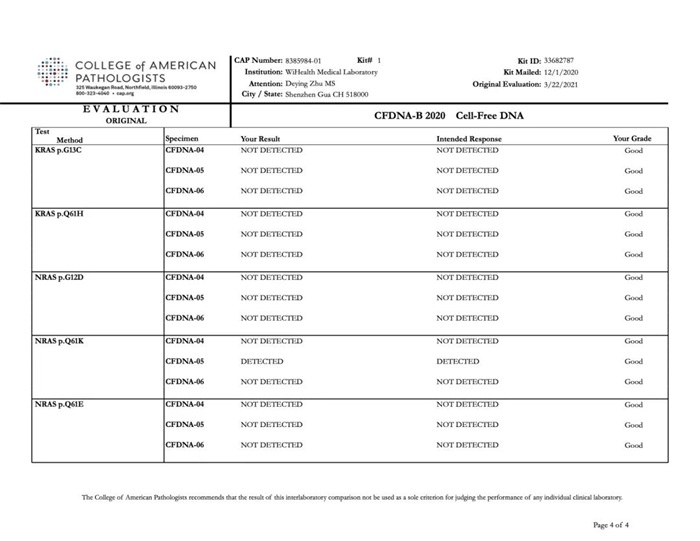
CAP认证是美国病理学家协会组织的临床实验质量认证计划,在全球被公认为是行业的“金标准”。裕策生物参与质检的所有检测结果均与CAP的官方标准答案完全一致。自2018年申请参加CAP室间质评以来,裕策生物已经连续多次满分通过CAP的室间质评,充分证明了裕策生物拥有过硬的技术实力、严谨的操作流程、卓越的产品设计。
未来,裕策生物将一如既往地保持国际一流水准,以更严格标准要求自身,继续积极参加国内及国际上各类质评考核,再接再厉、不断开拓,为医生和患者提供高质量的产品和专业的服务!
关于美国病理学家协会
美国病理学家协会(College of American Pathologists,CAP)是世界最大的病理学家组织,成立于1947年,被认为是国际上最具权威的临床检测实验室认可机构之一,也是被证明了的一种有效的同行评估模式,堪称为行业的国际“黄金标准”,FDA明确要求必须是来自CAP认证的实验室实验数据。CAP的一个重要内容就是向世界各地参与的实验室开展能力验证活动(Proficiency Testing,PT也称为室间质评)。
关于裕康医学实验室
深圳裕康医学检验实验室(简称:裕康医学实验室)是深圳市卫生健康委员会批准成立的第三方独立医学检验实验室。自建立之初,始终坚持质量先行的原则,按照美国病理学家协会(College of American Pathologists,CAP)、ISO15189准则等国际标准搭建实验室质量管理体系。
作为裕策生物旗下的医学检验实验室,裕康医学实验室始终贯彻科学、准确、严谨、创新的质量方针,以保障检测的准确性、可靠性和安全性,连续三年以优异成绩通过国家卫健委临检中心(NCCL)、美国病理学家协会(CAP)、欧洲分子基因诊断质量联盟(EMQN)等国内外权威机构的室间质评和能力验证项目。并于2021年1月获得CAP证书,跻身国际权威临检实验室行列。
裕康医学实验室拥有华大智造的DNBSEQ-T7基因测序仪、MGISEQ-2000基因测序仪、Illumina测序平台、NanoString空间组学平台、QuantStudio 3D数字PCR平台、qPCR平台、病理及免疫组化平台,建成从样本接收、样品管理、样本制备、上机测序、生信分析、结果解读、到报告发放的全流程信息化系统,同时能对基因信息数据库、临床解读数据库等进行实时更新,实现了数据分析和解读的全自动化。为临床提供高质量、高精度的临床检验服务,多维度、全方位的医学研究服务。
Copyright©2021
深圳裕策生物科技有限公司 版权所有
粤ICP备16128839号

