
近日,国家卫生健康委临床检验中心(NCCL)发布了《2020年肿瘤游离DNA基因突变高通量测序检测室间质量评价结果报告》,裕策生物旗下深圳裕康医学检验实验室(以下简称:裕康医学实验室)以满分成绩通过该类室间质评!
据了解,肿瘤游离 DNA(ctDNA)基因突变检测对肿瘤靶向治疗、早期治疗应答评估和耐药监测的实时评估等都具有一定的临床应用价值。由于组织样本的局限性,临床上逐渐开始使用患者血浆中的游离 DNA 进行肿瘤基因突变的检测。为了解临床实验室 ctDNA 基因突变检测的开展现状及质量状况,临检中心开展了该项目室间质量评价的预研,要求各临床实验室使用日常所用试剂和程序进行检测。
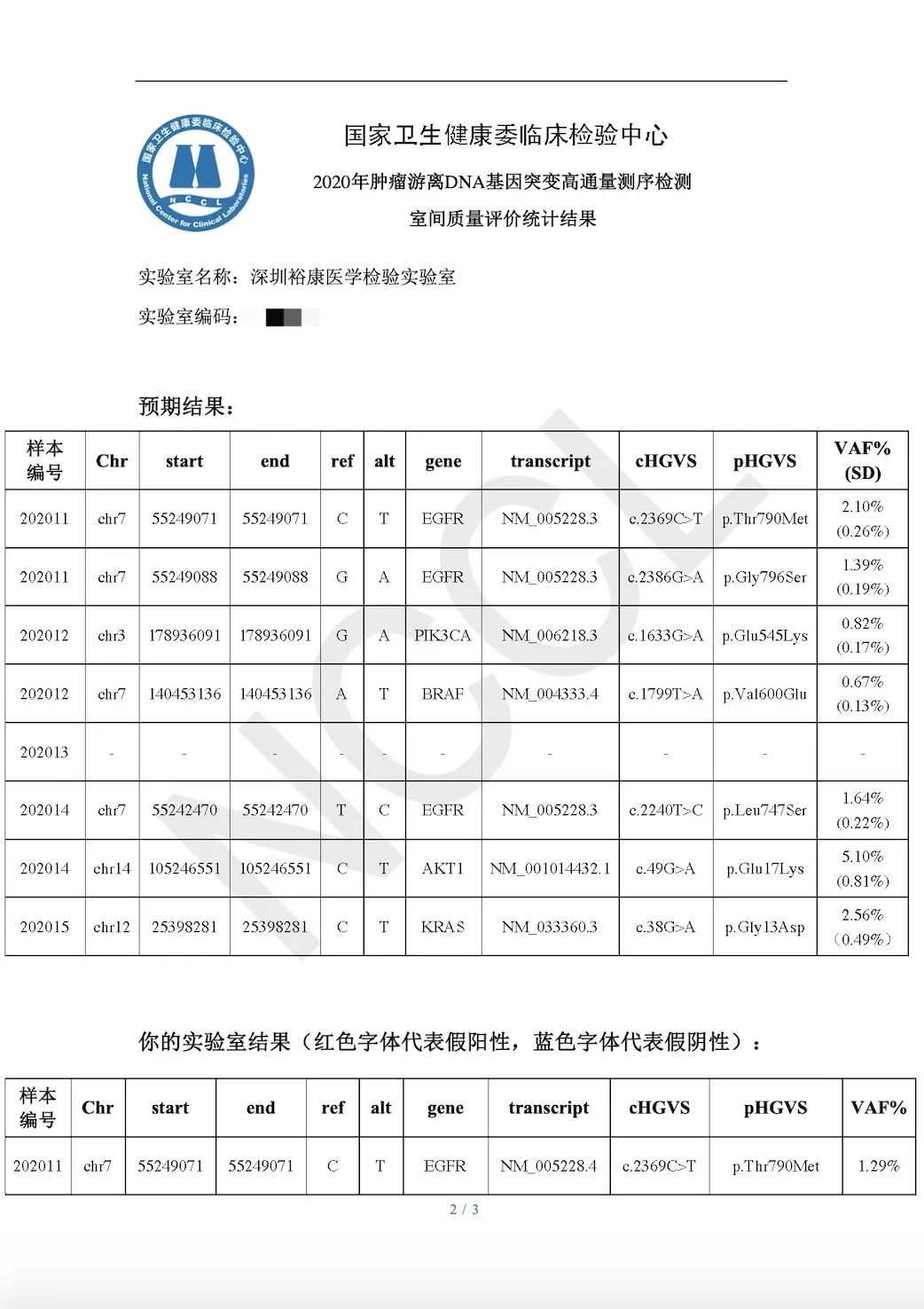
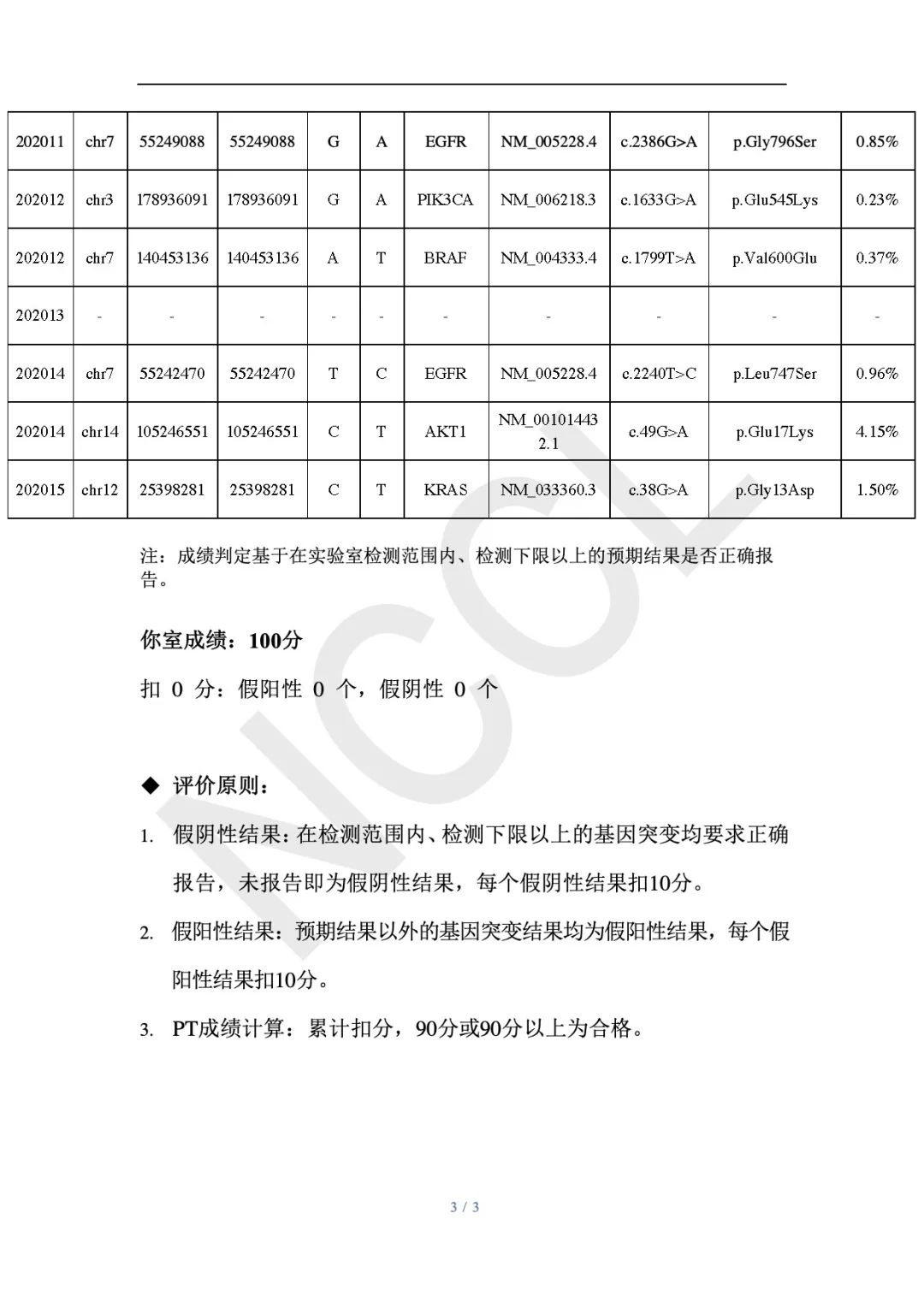
此次裕策生物上报的肿瘤游离DNA基因突变高通量测序检测范围包括:点突变、短片段插入缺失突变,以上涉及的所有基因突变类型均被裕策生物检出。
本次满分通过质评,裕策生物用实力证明了其在肿瘤游离DNA基因突变高通量测序检测方面的能力和专业性,也强有力地证明了裕策生物在操作规范、流程控制、质量监督等各个环节严格把关。未来,裕策生物会继续执行高标准、高要求的样品检测流程,为临床提供稳定可靠的检测服务。
关于国家卫生健康委临床检验中心
国家卫生健康委临床检验中心(NCCL),以临床检验质量控制与改进为主要工作方向,承担卫生部委托的全国临床检验质量管理与控制工作,运行全国临床检验室间质量评价计划,建立、应用临床检验参考系统,开展相关科学研究。
关于裕康医学实验室
裕康医学实验室占地1500平方米,是以临床需求为中心、以肿瘤精准免疫检测为特色、以精准用药为导向的综合检测中心。裕康医学实验室已经通过广东省临床检验中心临床基因扩增检验实验室技术审核,按照美国病理学家协会(CAP)及ISO9001质量管理体系建设并持续完善实验室质量管理体系,在生产中使用被严格验证过的SOP(标准操作流程),其中设立了包含从组织病理检测到报告解读全流程数十项质控点,保障每一份临床样本检测的准确性。目前,裕康医学实验室已经通过欧洲分子基因诊断质量联盟(EMQN)和国家卫生部临检中心组织的多项室间质评项目,充分证明裕康医学实验室的检测水平达到了国际一流水准,展现了其作为精准医疗行业领先企业的技术实力和完善的质量体系。
裕策生物近期获得的质量认证
2019年7月 通过CAP NGSST室间质评
2019年10月 通过德国莱茵TUV权威认证机构测评
2019年10月 通过NCCL室间质评
新闻|裕策生物通过2019全国实体瘤体细胞突变高通量测序检测室间质评
2019年10月 通过CAP EGFR室间质评
2019年11月 通过EMQN室间质评
新闻|裕策生物通过欧盟分子基因诊断质量联盟(EMQN)室间质评
2020年1月 通过CAP NGSST室间质评
2020年3月 通过EMQN室间质评
2020年5月 通过5项NCCL室间质评
2020年8月 通过CAP MTP室间质评
Copyright©2021
深圳裕策生物科技有限公司 版权所有
粤ICP备16128839号

